近日,国家传染病医学中心,复旦大学附属华山医院张文宏团队在感染病领域顶刊《Clinical Microbiology and Infection》上发表了一项关于新型口服抗流感药物ZX-7101A的2/3期临床数据,研究了这种药物在治疗单纯性成人流感中的安全性和有效性,该药物也有望成为流感明星药“玛巴洛沙韦”的国产版本。
国家传染病医学中心主任、复旦大学附属华山医院感染科主任张文宏教授、中国医学科学院北京协和医院急诊科主任朱华栋教授与复旦大学附属华山医院感染科艾静文教授共同牵头了此项研究,王红羽博士、王刚教授、高燕教授、屈莉红教授、王洪教授、邓敏教授及高海女教授为本文共同第一作者。

图形摘要:

一、研究背景
季节性流感导致全球5%-10%的成年人与20%-30%的儿童受感染,每年造成29万- 65万人死亡,死亡率为4.0-8.8/10万。目前,感染人类的流感病毒是甲型流感的H1N1和H3N2亚型,以及乙型流感的Victoria和Yamagata系。
美国食品和药物管理局(FDA)批准了几种抗流感病毒药物(见图1),新型帽依赖型核酸内切酶(CEN)抑制剂玛巴洛沙韦于2018年首次通过FDA批准上市。
ZX-7101A是新型CEN抑制剂ZX-7101的前药,与玛巴洛沙韦作用机制相同。临床前研究表明,ZX-7101A针对甲、乙型流感及高致病性禽流感有广谱抗病毒活性,其体外抗病毒活性与巴洛沙韦相当。I期临床研究表明,在40-160 mg剂量范围内,ZX-7101A药代动力学特征呈线性,t1/2为83.01~125.55。为了进一步研究ZX-7101A的有效性和安全性,开展了II/III期适应性设计研究。研究中,流感患者被随机分配,并分别服用ZX-7101A 40 mg、ZX-7101A 80 mg 或安慰剂。

图1:不同机制抗流感病毒药物
二、研究方法
本研究是一项多中心、随机、双盲、安慰剂对照的II/III期临床研究,以此评估ZX-7101A片对比安慰剂在成人无并发症单纯性流感受试者中的有效性和安全性。研究共分为两个阶段(图2),II期剂量探索阶段和III期疗效确证阶段,采用操作无缝适应性设计。

图2:研究设计图
三、研究结果
在这篇同时涵盖II期和III期的研究文献里,我们聚焦于样本量较大的三期研究结果进行解读。2023年2月-5月,本研究面向18-64岁单纯性流感患者展开招募,随机纳入723名受试者,经RT-PCR确诊,684例为流感患者,纳入ITTI人群。其中,甲型流感病毒感染率99.4%(680/684),H1N1亚型占54.8%(375/684),H3N2占43.6%(298/684)。
1、主要疗效终点——所有流感症状缓解时间
在ITTI人群中,ZX-7101A 40 mg、80 mg组及安慰剂组流感症状中位缓解时间分别为48.4h、39.4h、和62.9h,与安慰剂组相比,ZX-7101A两剂量组的所有流感症状缓解时间均显著缩短(40 mg组P=0.003;80 mg组P<0.001),且在体重≥80 kg和<80kg亚组患者中,症状缓解时间无明显差异,无需根据体重调整剂量。结果表明ZX-7101A能显著加快流感症状缓解,两剂量组较安慰剂组,能让受试者更早达到症状缓解标准。
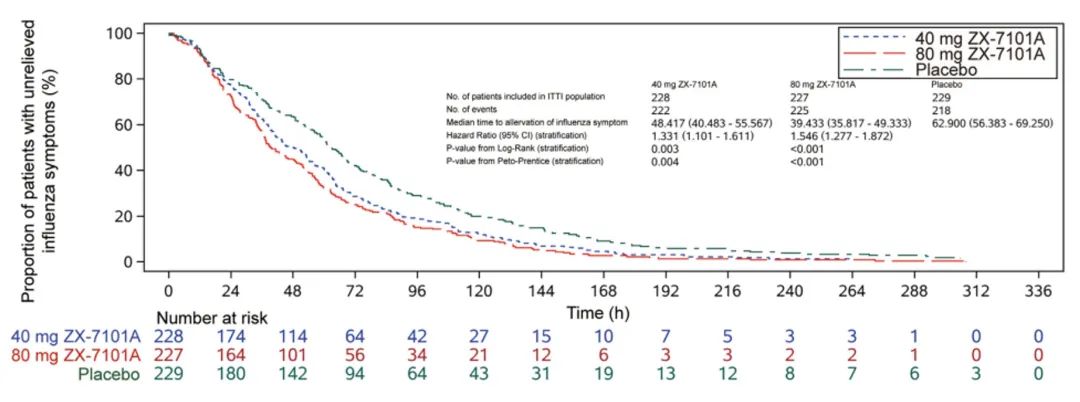
图3:III期试验中ZX-7101A与安慰剂在流感症状缓解时间方面的Kaplan-Meier曲线。各剂量组均单独与安慰剂组进行对比
2、次要疗效指标——病毒学指标
ZX-7101A 40 mg组、80 mg组的流感病毒RNA转阴时间分别为43.2h 和 41.4h,显著短于安慰剂组的90.78h。同样,与安慰剂组相比,ZX-7101A组病毒滴度中位检测时间显著缩短,且在治疗后24h、48h和96h,能检测到流感病毒RNA或病毒滴度的患者比例,也显著低于安慰剂组。
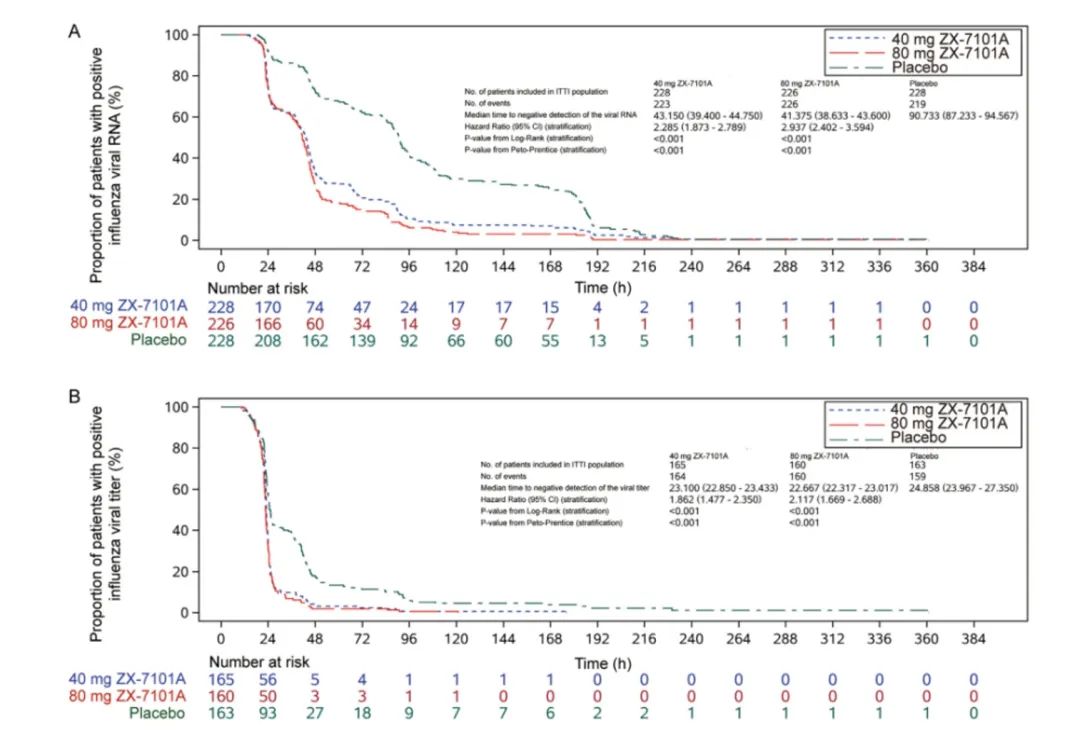
图4:在III期试验中,ZX-7101A与安慰剂对比,流感病毒RNA转阴时间(图A)和流感病毒滴度转阴时间(图B)的Kaplan-Meier曲线
3、安全性终点
在本项研究中,未发生导致死亡的不良事件。ZX-7101A 40mg组、80mg组不良事件发生率分别为41.8%、44.2%,在数值上均低于安慰剂组的53.8%。相比药物相关不良事件发生率,ZX-7101A 40mg组为7.1%,80mg组为9.2%,与安慰剂组的5.6%相近。治疗过程中,最常见的与治疗相关的不良反应为中性粒细胞计数和白细胞减少。综合上述研究结果,可表明ZX-7101A具有良好的安全性。
四、总结
单剂量口服ZX-7101A,能够有效减轻流感症状,快速降低病毒水平并清除病毒,且无需要根据体重调整剂量。同时安全性与安慰剂组相当,具有较好的安全性保障。
编辑: 杨丹纠错:171964650@qq.com

中国宁波网手机版

微信公众号